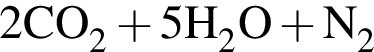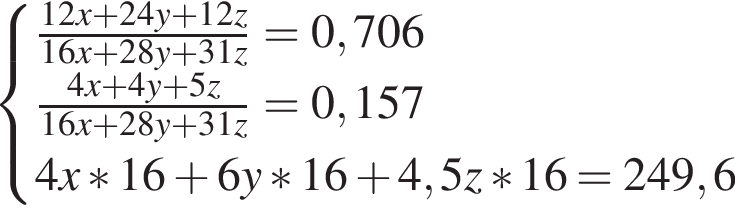Укажите формулу неорганического вещества:
1) 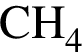
2) 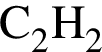
3) 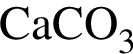
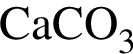
4) 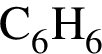
Решение. Все предложенные соединения — соединения, в состав которых входит углерод.
![]() ,
, ![]() ,
, ![]() — это органические соединения.
— это органические соединения. 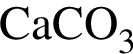 — это неорганическое соединение.
— это неорганическое соединение.
Несмотря на то, что все органические соединения — соединения, в состав которых входит углерод, карбонаты, в том числе 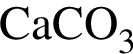 , к ним не относятся.
, к ним не относятся.
Правильный ответ указан под номером 3.
Ответ: 3
1101
3
Сложность: I

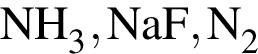
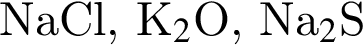
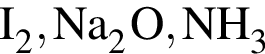
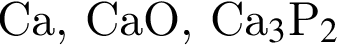
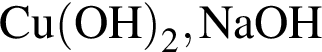
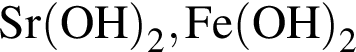
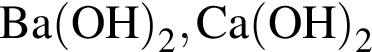
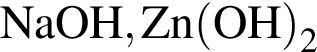
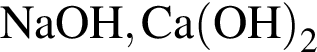
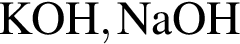
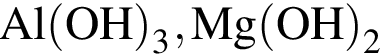
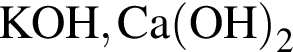
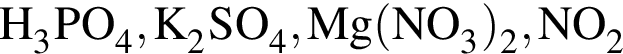 , с которыми реагирует разбавленный водный раствор
, с которыми реагирует разбавленный водный раствор 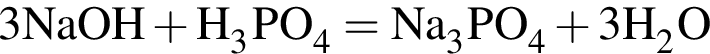
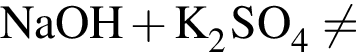
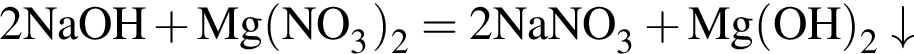
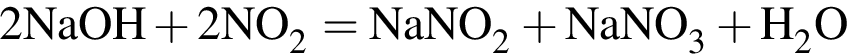

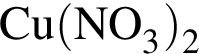
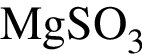
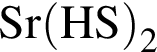
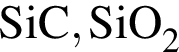 .
.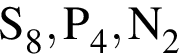 .
.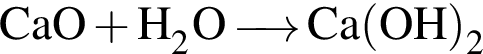
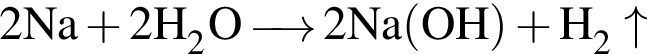
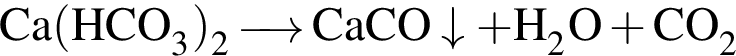
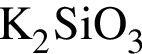
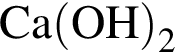
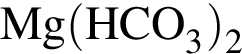
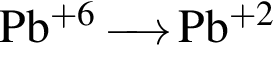
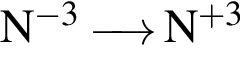
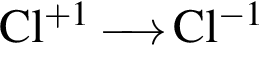
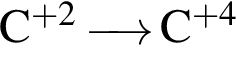
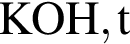
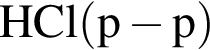
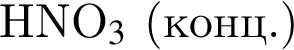
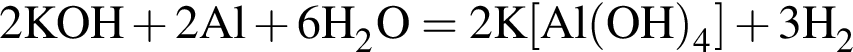
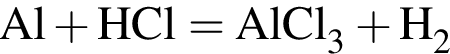

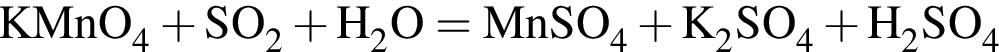 , равна:
, равна: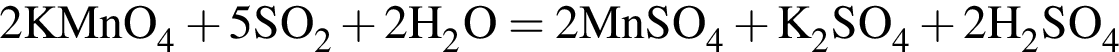
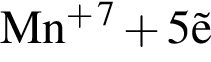 →
→ 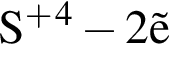 →
→ 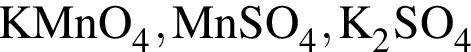 - вещества ионного строения,
- вещества ионного строения,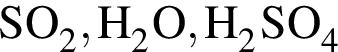 - вещества молекулярного строения.
- вещества молекулярного строения.
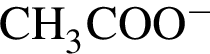
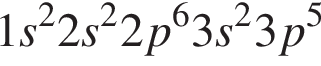 электронная конфигурация атома хлора в основном состоянии
электронная конфигурация атома хлора в основном состоянии находятся в низшей степени окисления
находятся в низшей степени окисления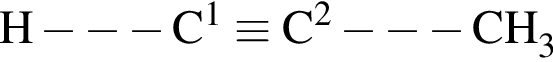 взаимодействует с избытком бромоводорода. При этом:
взаимодействует с избытком бромоводорода. При этом: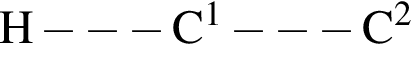 уменьшается
уменьшается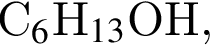 имеющих неразветвленный углеродный скелет, которые можно окислить до соответствующих карбоновых кислот состава
имеющих неразветвленный углеродный скелет, которые можно окислить до соответствующих карбоновых кислот состава 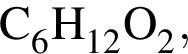 равно:
равно: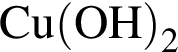
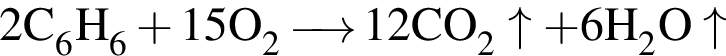 .
.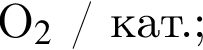
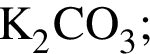
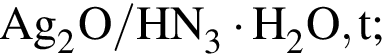
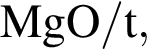 которые в указанных условиях способны превратить этаналь в этановую кислоту или ее соли, равно:
которые в указанных условиях способны превратить этаналь в этановую кислоту или ее соли, равно: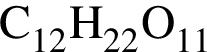
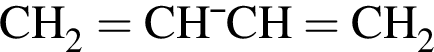
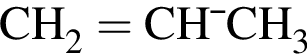
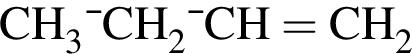
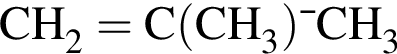

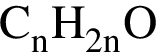
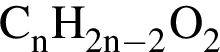
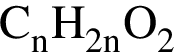
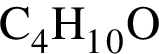 . Такую же формулу имеет бутанол-1.
. Такую же формулу имеет бутанол-1. 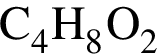 . Такую же формулу имеет бутановая кислота.
. Такую же формулу имеет бутановая кислота.
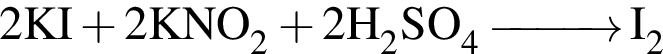 ↓
↓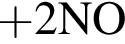 ↑
↑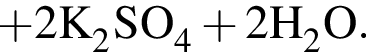
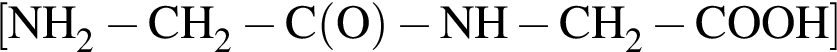 (М = (75 · 2)-18 = 132 г/моль) +
(М = (75 · 2)-18 = 132 г/моль) + 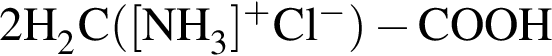 (М = 75+36.5 = 111.5 г/моль);
(М = 75+36.5 = 111.5 г/моль);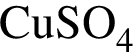 8% добавили медный купорос массой 80 г и перемешали смесь до полного его растворения. Рассчитайте массовую долю (%) соли в полученном растворе.
8% добавили медный купорос массой 80 г и перемешали смесь до полного его растворения. Рассчитайте массовую долю (%) соли в полученном растворе.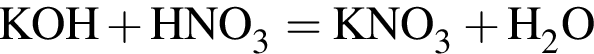
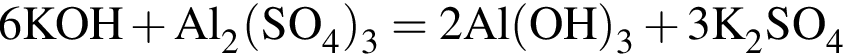
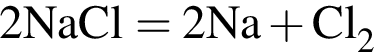 (зеленовато-жёлтый газ)
(зеленовато-жёлтый газ)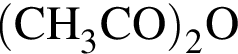 легко взаимодействует с водой, образуя уксусную кислоту:
легко взаимодействует с водой, образуя уксусную кислоту: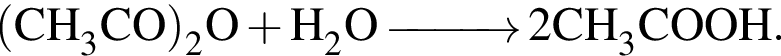
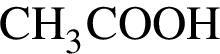 64% (
64% (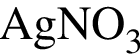 20%. Выпавший осадок отфильтровали, промыли, высушили и взвесили. Его масса оказалась равной 6,48 г. Вычислите массовую долю (%) ионов натрия в исходной смеси.
20%. Выпавший осадок отфильтровали, промыли, высушили и взвесили. Его масса оказалась равной 6,48 г. Вычислите массовую долю (%) ионов натрия в исходной смеси.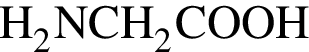
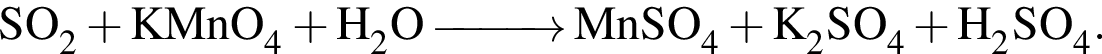

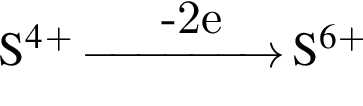
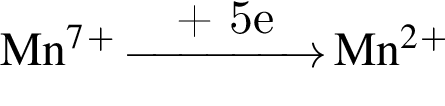
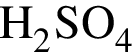 . Сумма коэффициентов перед ними: 5 + 2 + 2 = 9.
. Сумма коэффициентов перед ними: 5 + 2 + 2 = 9.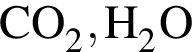 и
и 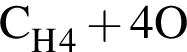 →
→ 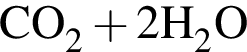
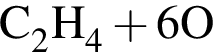 →
→ 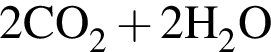
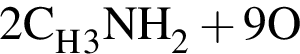 →
→